Arwydd (defnydd cymeradwy): Yn 2019, cymeradwyodd yr FDA ef ar gyfer trin anhwylder awydd rhywiol hypoweithredol cyffredinol (HSDD) a gafwyd mewn menywod cyn y menopos pan fydd y cyflwr yn achosi gofid amlwg ac nad yw oherwydd cyflyrau meddygol/seiciatrig eraill na sgîl-effeithiau cyffuriau.
Mecanwaith Gweithredu
Mae PT-141 yn agonist derbynnydd melanocortin (derbynnydd MC4 yn bennaf) sy'n modiwleiddio awydd rhywiol trwy lwybrau'r system nerfol ganolog.
Yn wahanol i atalyddion PDE5 (e.e., sildenafil), sy'n effeithio'n bennaf ar bibellau gwaed, mae PT-141 yn gweithio'n ganolog i effeithio ar gymhelliant rhywiol a chyffro.
Ffarmacoleg a Dosio
Gweinyddiaeth: Chwistrelliad isgroenol, yn ôl yr angen (ar alw).
Dos cymeradwy: 1.75 mg sc
Ffarmacocineteg:
Tmax ≈ ~60 munud
t½ ≈ 2–3 awr
Gall effeithiau bara sawl awr, mewn rhai adroddiadau hyd at ~16 awr.
Effeithiolrwydd Clinigol (Treialon Cyfnod III – RECONNECT, 24 wythnos, Treialon RCT)
Prif bwyntiau terfyn:
Mynegai Swyddogaeth Rhywiol Benywaidd–Parth Awydd (FSFI-D)
Graddfa Trallod Rhywiol Benywaidd (FSDS-DAO)
Canlyniadau allweddol (astudiaethau cronedig 301 + 302):
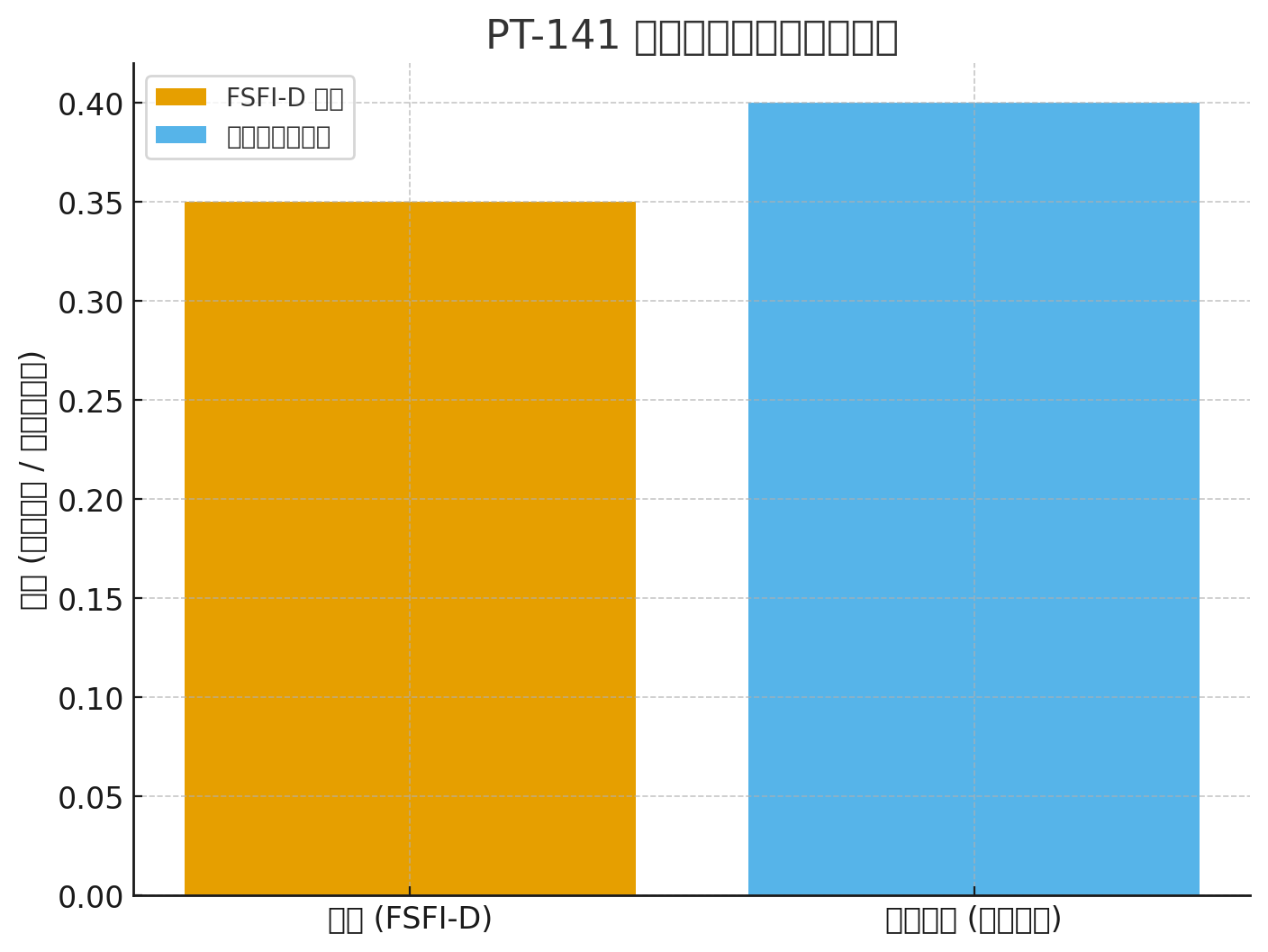
Gwelliant FSFI-D: +0.35 vs plasebo (P<0.001)
Gostyngiad sgôr FSDS-DAO: −0.33 vs plasebo (P<0.001)
Pwyntiau terfynol eraill: Roedd canlyniadau cefnogol (sgoriau swyddogaeth rywiol, boddhad a adroddwyd gan gleifion) yn tueddu'n gadarnhaol, ond nid oedd digwyddiadau rhywiol boddhaol (SSEs) bob amser yn dangos gwahaniaethau arwyddocaol cyson.
Digwyddiadau Niweidiol (a adroddir amlaf mewn treialon)
Cyffredin (≥10%):
Cyfog (~30–40%; hyd at ~40% wedi'i adrodd mewn treialon)
Fflysio (≥10%)
Cur pen (≥10%)
Effeithiau cardiofasgwlaidd:
Gwelwyd cynnydd dros dro mewn pwysedd gwaed a newidiadau yng nghyfradd y galon, a oedd fel arfer yn diflannu o fewn ychydig oriau.
Wedi'i wrthgymeradwyo neu ei ddefnyddio'n ofalus mewn cleifion â gorbwysedd heb ei reoli neu glefyd cardiofasgwlaidd.
Afu: Adroddiadau prin o gynnydd dros dro mewn ensymau afu; mae adroddiadau achos hynod brin yn awgrymu anaf acíwt i'r afu posibl, ond nid yw'n gyffredin.
Diogelwch Hirdymor (Astudiaeth Estynedig)
Canfu astudiaeth estyniad agored 52 wythnos welliannau cynaliadwy mewn awydd heb unrhyw arwyddion diogelwch mawr newydd.
Ystyrir bod proffil diogelwch hirdymor yn cael ei oddef yn dda ar y cyfan, gyda'r prif broblemau goddefgarwch yn dal i fod yn sgîl-effeithiau tymor byr fel cyfog.
Nodiadau Defnydd Allweddol
Mae'r boblogaeth gymeradwy wedi'i chyfyngu: Dim ond ar gyfer menywod cyn y menopos sydd â HSDD cyffredinol a gafwyd.
Heb ei gymeradwyo'n eang ar gyfer dynion (mae ED neu awydd isel mewn dynion yn parhau i fod yn destun ymchwiliad).
Mae sgrinio diogelwch yn hanfodol: Dylid asesu gorbwysedd, clefyd cardiofasgwlaidd, a hanes yr afu cyn rhagnodi.
Crynodeb Data Cyflym
Cymeradwyaeth FDA: 2019 (Vyleesi).
Dos: pigiad isgroenol o 1.75 mg, ar alw.
PK: Tmax ~60 mun; t½ 2–3 awr; effeithiau hyd at ~16 awr.
Effeithiolrwydd (Cyfnod III, wedi'i gronni):
FSFI-D: +0.35 (P<.001)
FSDS-DAO: −0.33 (P<.001)
Digwyddiadau niweidiol:
Cyfog: hyd at ~40%
Fflysio: ≥10%
Cur pen: ≥10%
Nodwyd cynnydd dros dro mewn pwysedd gwaed.
Tabl a Graff Cymharol (Crynodeb)
| Astudiaeth / Math o Ddata | Pwynt Terfynol / Mesur | Gwerth / Disgrifiad |
|---|---|---|
| Cyfnod III (301+302 wedi'u cronni) | FSFI-D (parth awydd) | +0.35 vs plasebo (P<0.001); FSDS-DAO −0.33 |
| Digwyddiadau Niweidiol | Cyfog, cochni, cur pen | Cyfog ~30–40% (uchafswm ~40%); ffrwsh ≥10%; cur pen ≥10% |
Amser postio: Medi-30-2025